“…ที่ผ่านมาวัคซีนโควิดที่พัฒนาโดยคนไทยยังอยู่ในขั้นตอนของการทดลอง ขณะที่เริ่มมีวัคซีนจากผู้ผลิตจากต่างประเทศหลายรายออกสู่ตลาดแล้ว แต่ความพยายามนี้ไม่สูญป่าว ไทยมีวัคซีนที่ผลิตเองได้ นับเป็นก้าวสำคัญของการพึ่งพาตนเอง และเป็นการทดสอบความพร้อมรับมือกับโรคระบาดอื่นๆ ที่อาจจะเข้ามาในอนาคต…”
……………………………………………………………..
วัคซีนต้านโควิด เป็นเครื่องมือหนึ่งในการควบคุมสถานการณ์การแพร่ระบาดของโควิด เป็นความหวังที่จะฟื้นฟูเศรษฐกิจและสังคมภายในประเทศให้ดียิ่งขึ้น เนื่องจากแพทย์ภายในกระทรวงสาธารณสุขต่างให้คำแนะนำตามหลัก ‘ภูมิคุ้มกันหมู่’ หรือ Herd Immunity ว่า หากเมื่อใดที่ประชากรภายในประเทศไทยได้รับวัคซีน 50 – 60% การแพร่ระบาดของเชื้อโควิดจะลดลงอย่างมาก และประชาชนจะสามารถเข้าสู่วิถีชีวิตปรกติได้อีกครั้งภายในระยะเวลาที่เร็วขึ้น หลังจากที่ทั่วทั้งประเทศและทั่วโลกมีภูมิต้านทานของโรคโควิดในระดับสูงแล้ว
ปัจจุบันไทยมีวัคซีนต้านโควิดของต่างประเทศ ที่ได้รับการอนุมัติจากสำนักงานคณะกรรมการอาหารและยา (อย.) และถูกนำมาใช้อยู่ด้วยกัน 3 ยี่ห้อ ได้แก่ วัคซีนซิโนแวค ของบริษัท ซิโนแวค จากประเทศจีน, วัคซีนแอสตร้าเซนเนก้า ของบริษัท แอสตร้าเซนเนก้า จากสหราชอาณาจักร และวัคซีนจอห์นสันแอนด์จอห์นสัน บริษัท จอห์นสันแอนด์จอห์นสัน จากสหรัฐอเมริกา ซึ่งขณะนี้รัฐจัดหาได้แล้วประมาณ 75 ล้านโดส เพียงพอให้กับประชาชน 35 ล้านคน ยังขาดวัคซีนอีก 10 ล้านโดส เพื่อฉีดให้กับประชาชนอีก 5 ล้านคน ถึงจะเพียงพอต่อการเกิด ‘ภูมิคุ้มกันหมู่’ ซึ่งรัฐได้ไฟเขียวให้โรงพยาบาลเอกชนได้เสนอตัวนำเข้าวัคซีน เพื่อเป็นทางเลือกให้กับประชาชนแล้ว
อย่างไรก็ตาม การพึ่งพาวัคซีนต้านโควิดจากต่างประเทศ เป็นความไม่แน่นอนว่าจะได้รับวัคซีนได้ตรงกำหนดเวลาหรือไม่ และไม่สามารถต่อรองราคาสั่งจองวัคซีนได้มาก เนื่องจากขณะนี้ตลาดยังเป็นของผู้ขาย ดังนั้นแล้วหากไทยสามารถพึ่งพาตนเองได้ด้วยการผลิตวัคซีนใช้เองภายในประเทศ ความหวังในการควบคุมโรคก็อาจมีประสิทธิภาพมากขึ้น
ที่ผ่านมาวัคซีนโควิดที่พัฒนาโดยคนไทยยังอยู่ในขั้นตอนของการทดลอง โดยมีวัคซีนที่ไทยผลิตเอง ดังนี้
วัคซีนโควิด 19 ชนิดเชื้อตาย จากองค์การเภสัชกรรมร่วมกับคณะเวชศาสตร์เขตร้อน มหาวิทยาลัยมหิดล ซึ่งอยู่ระหว่างทดลองในมนุษย์ระยะที่ 1 และระยะที่ 2
วัคซีน ChulaCov19 จากศูนย์วิจัยวัคซีน คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ซึ่งอยู่ระหว่างการเตรียมความพร้อมทดลองในมนุษย์ระยะที่ 1 ในเดือน พ.ค.2564
นับเป็นก้าวสำคัญของการพึ่งพาตนเอง และเป็นการทดสอบความพร้อมรับมือกับโรคระบาดอื่นๆ ที่อาจจะเข้ามาในอนาคต
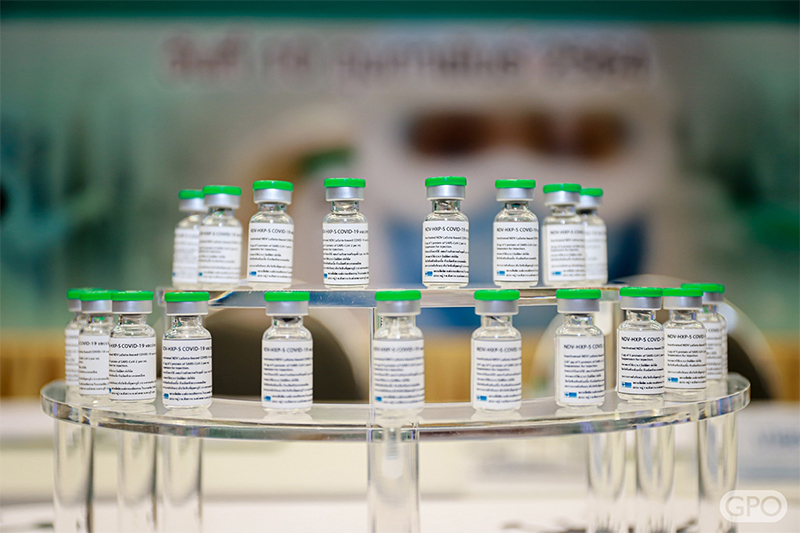 วัคซีนโควิด19 ชนิดเชื้อตาย
วัคซีนโควิด19 ชนิดเชื้อตาย
@ อภ. ทดลอง‘วัคซีนผลิตเอง’ ในมนุษย์แล้ว คาดปลายปีได้สูตรที่ดีที่สุด
ปัจจุบันองค์การเภสัชกรรม (อภ.) ร่วมมือกับสถาบัน PATH ประเทศสหรัฐอเมริกา พันธมิตรในต่างประเทศ ซึ่งเป็นองค์กรที่มุ่งพัฒนาให้มีวัคซีนคุณภาพดี ราคาไม่แพง เพิ่มการเข้าถึงวัคซีนของประชาชนภายในประเทศรายได้ปานกลางถึงรายได้ต่ำให้มีวัคซีน ผลิต ‘วัคซีนต้านโควิด19 ชนิดเชื้อตาย’ ด้วยเทคโนโลยีไข่ไก่ฟัก ซึ่งผ่านการทดลองในสัตว์พบว่ากระตุ้นภูมิคุ้มกันได้ผลดีและปลอดภัย รวมถึงยังสามารถผลิตได้ปริมาณมากในระยะเวลาสั้น และมีความเสถียรมากในระหว่างการเก็บรักษา และการขนส่ง
“ขณะนี้ได้เริ่มวิจัยในมนุษย์ระยะที่ 1 และ 2 จำนวน 460 คน โดยเมื่อวันที่ 22 มี.ค.2564 ที่ผ่านมา ได้เริ่มประเดิมฉีดอาสาสมัครกลุ่มแรกไปแล้ว 18 ราย ยังไม่พบผลข้างเคียงอันไม่พึงประสงค์รุนแรงจากวัคซีน คาดปลายปีนี้จะได้สูตรวัคซีนที่ดีที่สุดเพื่อนำไปศึกษาต่อในระยะที่ 3 และคาดว่าในปี 2565 จะยื่นขอทะเบียนตำรับและผลิตในอุตสาหกรรมได้” นพ.วิฑูรย์ ด่านวิบูลย์ ผู้อำนวยการองค์การเภสัชกรรม กล่าว
วัคซีนโควิด ของ อภ.นั้น เป็นวัคซีนชนิดเชื้อตาย ด้วยการใช้เทคโนโลยีไข่ไก่ฟัก อันเป็นเทคโนโลยีหลักที่ได้ใช้กันมาอย่างยาวนาน และได้รับความนิยมในการผลิตวัคซีนป้องกันโรคไข้หวัดใหญ่
โดยในการผลิตวัคซีนนั้น อภ. ได้รับหัวเชื้อไวรัสตั้งต้นจากสถานบัน PATH ที่ถูกพัฒนาโดยโรงเรียนแพทย์ Mount Sinai ในนิวยอร์ก และมหาวิทยาลัยเท็กซัส เพื่อให้ในการวิจัยพัฒนาวัคซีนตั้งแต่ปี 2563 ซึ่งหัวเชื้อไวรัสตั้งต้นมีการตัดแต่งพันธุกรรมไวรัสนิวคาสเซิล ให้มีโปรตีนส่วนหนาม (Spike protein) ของไวรัสโควิด จึงมีความปลอดภัยไม่ก่อให้เกิดโรค เพิ่มจำนวนในไข่ไก่ฟักได้ ซึ่งองค์การเภสัชกรรมมีเทคโนโลยีนี้ในการผลิตวัคซีนไข้หวัดใหญ่มาก่อน
นพ.วิฑูรย์ กล่าวเพิ่มเติมว่า จากการทดสอบความเป็นพิษในหนูแรท (Rats) ที่ประเทศอินเดีย พบว่าวัคซีนมีความปลอดภัย และการทดสอบประสิทธิภาพ (Challenge study) ในหนูแฮมสเตอร์ (Hamsters) ที่ประเทศสหรัฐอเมริกา พบผลเบื้องต้นพบว่า วัคซีนมีประสิทธิภาพในการป้องกันโรคจากการติดเชื้อโควิด สอดคล้องกับผลการศึกษาความสามารถในการกระตุ้นภูมิคุ้มกัน ที่พบว่าวัคซีนสามารถกระตุ้นภูมิคุ้มกันต่อโปรตีนหนามของไวรัสโคโรนาได้ดี
ส่วนในประเด็นเรื่องเชื้อกลายพันธุ์นั้น นพ.วิฑูรย์ กล่าวว่า องค์การเภสัชกรรม ได้รับความร่วมมือจากศูนย์พันธุวิศวกรรมและเทคโนโลยีชีวภาพแห่งชาติ สวทช. ภายใต้การดูแลของ ดร.อนันต์ จงแก้ววัฒนา ได้ทำการทดสอบวัคซีนองค์การเภสัชกรรมในการต้านเชื้อกลายพันธุ์ โดยเฉพาะเชื้อไวรัสโควิด สายพันธุ์แอฟริกาใต้ (B.1.351) ที่ทางการแพทย์มีความเป็นกังวลต่อสายพันธุ์ดังกล่าวมากด้วย
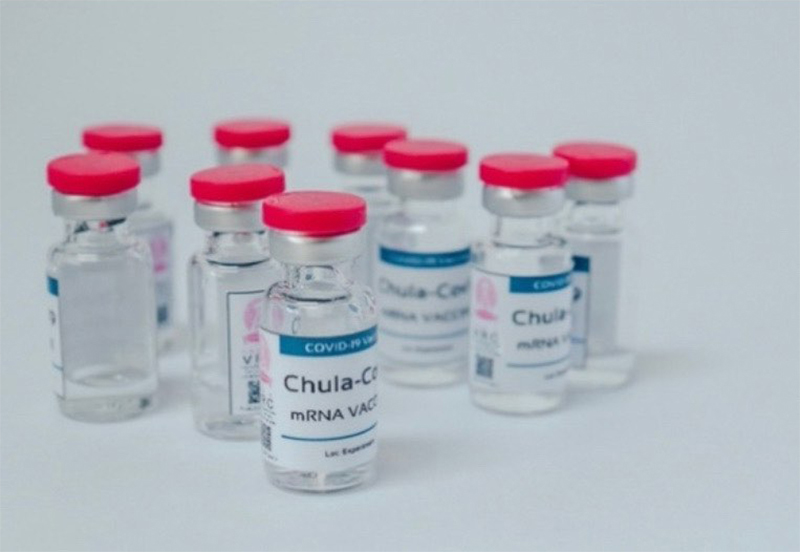 วัคซีนChulaCov19
วัคซีนChulaCov19
@ วัคซีนจุฬาฯ เตรียมทดลองในมนุษย์ พ.ค. 64
ขณะเดียวกัน คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ได้เปิดเผยความคืบหน้าการพัฒนาการผลิตวัคซีนต้านโควิด ที่มีชื่อว่า ‘ChulaCov19’ ซึ่งอยู่ระหว่างการเตรียมความพร้อมทดลองในมนุษย์ระยะที่ 1 ในเดือน พ.ค.2564 และขณะนี้กำลังเตรียมพัฒนาวัคซีนรุ่นที่ 2 เพื่อต้านเชื้อโควิดกลายพันธุ์ด้วย
นับเป็นอีก 1 ข่าวดีของวงการสาธารณสุขไทยที่คนไทยจะได้รับวัคซีน ChulaCov19 ชนิด mRNA ที่พัฒนาโดยทีมคณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ร่วมกับ บริษัท ไบโอเนท-เอเชีย จำกัด หลังจากพบผลการทดลองฉีดวัคนซีนต้านโควิดในหนูและลิง สามารถกระตุ้นภูมิคุ้มกันในระดับสูง โดยป้องหนูไม่ให้ป่วยได้ 100% และยับยั้งไม่ให้เชื้อเข้าสู่กระแสเลือดได้ 100% เมื่อได้รับวัคซีน 2 เข็ม ห่างกัน 3 สัปดาห์ นอกจากนี้วัคซีน ChulaCov19 ยังสามารถเก็บในอุณหภูมิตู้เย็นปกติคือ 2-8 องศาเซลเซียส ได้อย่างน้อย 1 เดือนด้วย และกำลังรอผลวิจัยที่ 3 เดือน ดังนั้นจึงไม่มีปัญหาเรื่องการขนส่งกระจายวัคซีนไปยังจังหวัดต่างๆ ทั่วประเทศ
ด้าน ศ.นพ.เกียรติ รักษ์รุ่งธรรม ผู้อำนวยการบริหารโครงการพัฒนาวัคซีน covid19 ศูนย์วิจัยวัคซีนคณะแพทย์ศาสตร์จุฬาฯ กล่าวว่า ในการทดลองในมนุษย์ระยะที่ 1 ที่จะเริ่มในเดือน พ.ค.2564 จะใช้เวลาประมาณ 2 เดือน ซึ่งน่าจะเสร็จประมาณต้นเดือน ก.ค.2564 และจะเริ่มทดลองระยะ 2 ต่อไป ซึ่งจะใช้อาสาสมัคร 300-600 คน ส่วนระยะที่ 3 นั้น เนื่องจากอยู่ในรายชื่อกรรมการวิจัยวัคซีนขององค์การอนามัยโลกด้วย ซึ่งมีการตั้งคณะกรรมการวิเคราะห์ข้อมูลวัคซีนทั้งหลายในโลกว่าสามารถกระตุ้นภูมิคุ้มกันได้มากน้อยแค่ไหน ซึ่งจะทราบผลอีก 6 เดือน ถ้าทราบผลแล้ว โดยเฉพาะวัคซีน mRNA ตัวอื่นๆ หากพบว่ากระตุ้นภูมิได้ดี วัคซีน ChulaCov19 อาจไม่ต้องทำการทดลองในระยะที่ 3 แต่ต้องทดลองระยะ 2B กับกลุ่มตัวอย่าง 5,000 คน แน่นอน เพื่อดูความปลอดภัยรอบสุดท้าย
สำหรับการพัฒนาวัคซีนรุ่น 2 เพื่อป้องกันเชื้อโควิดกลายพันธุ์ ศ.นพ.เกียรติ กล่าวด้วยว่า วัคซีนชนิด mRNA นั้นสามารถปรับปรุงให้เข้ากับเชื้อโรคได้ ซึ่งขณะนี้อยู่ระหว่างการทำวัคซีนสูตรคอกเทล คือป้องกัน 3 สายพันธุ์ ทั้งสายพันธุ์ดั้งเดิม สายพันธุ์ที่มีการกลายพันธุ์ในอังกฤษ และสายพันธุ์ที่มีการกลายพันธุ์ในแอฟริกาใต้ หรืออาจจะเป็นสูตรผสม 2 สายพันธุ์ เป็นต้น ทั้งนี้จะเริ่มดำเนินการในสัตว์ทดลอง ภายใน 2 เดือน โดยทำควบคู่ไปกับการทดลองวัคซีนรุ่นแรกในคนระยะที่ 1-2
“เมื่อทุกอย่างสำเร็จ โรงงานผลิตวัคซีนของไบโอเนท-เอเชีย จะสามารถผลิตวัคซีนได้อย่างครบวงจร วิกฤตรอบใหม่นี้จะทำให้เราสามารถปิดช่องว่างวงจรการผลิตวัคซีนในประเทศไทยได้ ถ้าในการทดลองวัคซีนรุ่นที่1 ยังไม่ทัน ก็หวังว่าการพัฒนาวัคซีนรุ่นที่ 2 จะปิดช่องว่างได้” ศ.นพ.เกียรติ กล่าว
 สารตั้งต้นยาฟาวิพิราเวียร์
สารตั้งต้นยาฟาวิพิราเวียร์
@ ไทยสังเคราะห์สารตั้งต้นยา ‘ฟาวิพิราเวียร์’ แทนการนำเข้าจากต่างประเทศ
นอกจากวัคซีนต้านโควิดแล้วนั้น ไทยยังสามารถผลิตสารตั้งต้นในการผลิตยาต้านโควิดได้เอง ด้วยความร่วมมือขององค์การสัชกรรม (อภ.) กับสำนักงานพัฒนาวิทยาศาสตร์และเทคโนโลยีแห่งชาติ (สวทช.) ที่ทำการวิจัยและพัฒนายารักษาผู้ติดเชื้อโควิด หรือที่เรียกกันว่า ‘ยาฟาวิพิราเวียร์’ หลังจากที่อุตสาหกรรมการผลิตยาของประเทศไทยอยู่ในระดับปลายน้ำ ต้องนำเข้าสารออกฤทธิ์ทางยา หรือ Active Phrmaceutical Ingredients (API) ซึ่งเป็นสารตั้งต้นในหารผลิตยารักษาโรคต่างๆ จากต่างประเทศมากถึง 95%
โดยเมื่อวันที่ 3 มี.ค.2564 ที่ผ่านมา ดร.ณรงค์ ศิริเลิศวรกุล ผู้อำนวยการสำนักงานพัฒนาวิทยาศาสตร์ และ นพ.วิฑูรย์ ด่านวิบูลย์ ผู้อำนวยการองค์การเภสัชกรรม ได้ร่วมแถลงข่าวกรณีสามารถสังเคราะห์สารออกฤทธิ์ตั้งต้นของยาต้านโควิด ‘ยาฟาวิพิราเวียร์’ ทดแทนวัตถุดิบนำเข้าจากต่างประเทศได้สำเร็จ
“การประสบความสำเร็จในการพัฒนาวัตถุดิบสารออกฤทธิ์ทางยา เป็นนิมิตหมายที่ดีที่ของประเทศไทยที่สามารถพัฒนาอุตสาหกรรมวัคซีน ยา รวมถึงอุตสาหกรรมอื่นๆ ที่จะช่วยรับมือต่อวิกฤติโรคระบาดในอนาคต ทำให้ประเทศมีความเข้มแข็งทางด้านการแพทย์และสาธารณสุข สามารถพึ่งพาตนเองได้ ลดการนำเข้า ซึ่งเป็นแนวทางที่ช่วยให้ประเทศไทยสามารถก้าวพ้นกับดักรายได้ปานกลาง เพราะเราไม่ได้มีแค่วิทยาการความรู้ แต่เรายังสามารถผลิตเพื่อการส่งขายได้อีกด้วย” ดร.ณรงค์ กล่าว
สำหรับขั้นตอนต่อไปนั้น นพ.วิฑูรย์ กล่าวว่า องค์การเภสัชกรรม จะร่วมกับทีมนักวิจัย ไบโอเทค สวทช. ขยายการผลิตในระดับกึ่งอุตสาหกรรม (Pilot Scale) และจะมีการขยายผลไปสู่อุตสาหกรรม API โดยมี บริษัท ปตท. จำกัด (มหาชน) ร่วมศึกษาความเป็นไปได้ เพื่อขยายผลสู่ขั้นตอนการผลิตในเชิงพาณิชย์ต่อไป ทั้งนี้จะมีการศึกษาความเป็นไปได้ในการสร้างโรงงานสังเคราะห์วัตถุดิบยาฟาวิพิราเวียร์และวัตถุดิบยาจำเป็นอื่นๆด้วย เพื่อส่งเสริมและพัฒนาวัตถุดิบยาที่มีความจำเป็นต่อระบบสาธารณสุข และมีศักยภาพในเชิงพาณิชย์ สร้างความมั่นคงทางยาให้กับประเทศไทย
(ภาพจาก : องค์การเภสัชกรรม และคณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย)
#กดคลิก ติดตาม ส่งแชร์ข่าวอิศรา ได้ที่นี่ https://www.facebook.com/isranewsfanpage



 Isranews Agency | สำนักข่าวอิศรา
Isranews Agency | สำนักข่าวอิศรา