ได้รายงานผู้ป่วยเด็ก 1 ราย ซึ่งเข้ารับการรักษาด้วยอาการ cardiogenic shock และ mitral insufficiency จากการตรวจทางห้องปฏิบัติการพบว่าผู้ป่วยมีการติดเชื้อ M. pne umoniae และสาเหตุของ mitral insufficiency เกิดจาก การมี papillary muscle dysfunction จากการมีทำลายต่อ กล้ามเนื้อหัวใจ ดังนั้นในผู้ป่วยที่มีอาการของหัวใจวายเฉียบพลันร่วมกับ mitral insufficiency จําเป็นต้องคิดถึงสาเหตุ จากการติดเชื้อ M. pneumoniae นอกเหนือจากไข้รูมาติก กล้ามเนื้อหัวใจอักเสบจากเชื้อไวรัส และ การติดเชื้อที่ลิ้นหัวใจ
หมายเหตุสำนักข่าวอิศรา (www.isranews.org) : เป็นบทความวิชาการเรื่องของ นพ.ไพโรจน์ โชติวิทยธารากรและคณะ
การติดเชื้อ Mycoplasma pneumoniae ทําให้เกิดอาการทางระบบทางเดินหายใจ เช่น ปอดบวม หลอดลม อักเสบ และมีภาวะแทรกซ้อนต่าง ๆ เช่น erythema multi- forme, เยื่อหุ้มสมองอักเสบ ประสาทส่วนปลายอักเสบ ภาวะ ซีดจากเม็ดโลหิตแดงแตก ตับอักเสบ กล้ามเนื้อหัวใจอักเสบ หรือ perimyocarditis myocarditis เป็นต้น (1,2,3) อาการ cardiogenic shock พบได้น้อยมาก ผู้รายงานได้รายงานผู้ ป่วยเด็ก 1 ราย ซึ่งเข้ารับการรักษาด้วยอาการ cardiogenic shock ร่วมกับ mitral insufficiency จากการติดเชื้อ Mycop lasma pneumoniae โดยมีวัตถุประสงค์เพื่อให้แพทย์ได้คิด ถึงการติดเชื้อ Mycoplasma pneumoniae ในการวินิจฉัย แยกโรคผู้ป่วยที่มีอาการ cardiogenic shock ร่วมกับ mitral insufficiency นอกเหนือจากกล้ามเนื้อหัวใจอักเสบจากเชื้อ ไวรัส การติดเชื้อที่ลิ้นหัวใจและ rheumatic carditis.
รายงานผู้ป่วย
ผู้ป่วยเด็กชายไทยอายุ 14 ปี เข้ารับการรักษาใน ภาควิชากุมารเวชศาสตร์ โรงพยาบาลจุฬาลงกรณ์ ด้วยอาการ ของ ไข้ ไอ และหายใจหอบ ในวันที่เข้ารับการรักษา ในโรง พยาบาล โดยมีประวัติของการมีอาการไอแห้ง ๆ อาเจียน และ ปวดบริเวณน่องทั้งสองข้าง เป็นมา 4 วันก่อนมาโรงพยาบาล อดีตผู้ป่วยเป็นเด็กที่แข็งแรงดีมาตลอด และไม่มีประวัติของโรคหัวใจมาก่อน
การตรวจร่างกายแรกรับ พบว่าผู้ป่วย ซีด, poor tissue perfusion, หายใจหอบ, อุณหภูมิของร่างกาย 38 องศาเซลเซียส ความดัน 80/60, ชีพจร 130 ครั้ง/นาที, หายใจ 35 ครั้งต่อนาที, Central venous pressure 18 เซนติเมตร ตาเหลืองเล็กน้อย คอไม่แดงและไม่มี exudate, ตรวจปอด พบ fine crepitation ที่บริเวณฐานของปอดทั้งสองข้าง, การ ตรวจหัวใจและหลอดเลือดพบผู้ป่วยมีเส้นเลือดต่ำที่คอโป่ง, PMI อยู่ที่บริเวณช่องซี่โครงคู่ที่ 5 ห่างจาก left midclavi-cular line 1 เซนติเมตร เสียง 1 และ 2 ปกติ พบมี S3 gallop, ejection systolic murmur grade 2-3/6 ที่บริเวณ apex กระจายไปยังรักแร้ และ ejection systolic click ที่ บริเวณ pulmonary valve ตับโต 4 เซนติเมตรต่ำกว่าใต้ ชายโครงขวา ตรวจไม่พบม้ามและการตรวจทางระบบประสาท อยู่ในเกณฑ์ปกติ
การตรวจทางห้องปฏิบัติการพบว่าฮีโมโกลบิน 7.9 %กรัม 2 เม็ดเลือดขาว 14900 เซลล์/ลบ.มม. นิวโทรฟิล 87% โมโนนิวเคลียเซลล์ 2 ลิมโฟไซท์ 11% Reticulocyte 8.2% NRBC 5/100 เม็ดเลือดขาว เกร็ดเลือด 285,000 BUN 34 มก.% creatinine 0.3 มก% น้ำตาล 62 ม.% Blood gas pH 7.253 PCO2, 28.6 มม. ปรอท PO2 73.1 มม. ปรอท BE - 12.6 HCO3 12.2 mEq/L บิลิรูบิน 1.6 มก.% Direct bilirubin 0.8 มก. % Alkaline phospha tase 43 หน่วยสากล Serum aspatate aminotrasferase 2660 หน่วยสากล Serum alanine aminotransferase 8220 หน่วยสากล Creatine phosphokinase 572 หน่วย สากล, lactic dehydragenase 1170 หน่วยสากล ESR 35 มม./ชม. CRP 2 + G6-PD ปกติ Coomb's test ให้ ผลลบทั้ง direct และ indirect การเพาะเชื้อจากเลือด และคอให้ผลลบ
การตรวจน้ำเหลือง สําหรับการติดเชื้อสเตรปโต คอคัส พบ ASO ไตเตอร์ 1 : 195 (ปกติ < 1 : 244), antiDNase B 1 : 300 (ปกติ < 1 : 300) และการตรวจอีก 2 สัปดาห์ พบ ASO และ anti DNase มีค่าเป็น 1:100 และ 1 : 300 ตามลําดับ แต่พบว่าการตรวจ cold agglutenin (CA) 1 : 256 และ complement fixation (CF) 1 : 64 ในวันที่เข้า รับการรักษาและเพิ่มขึ้นเป็น 1 : 256 ทั้ง CA และ CF ใน อีก 2 สัปดาห์ต่อมา และการตรวจแอนติบอดี้ต่อ Coxsackie B ให้ผลลบ
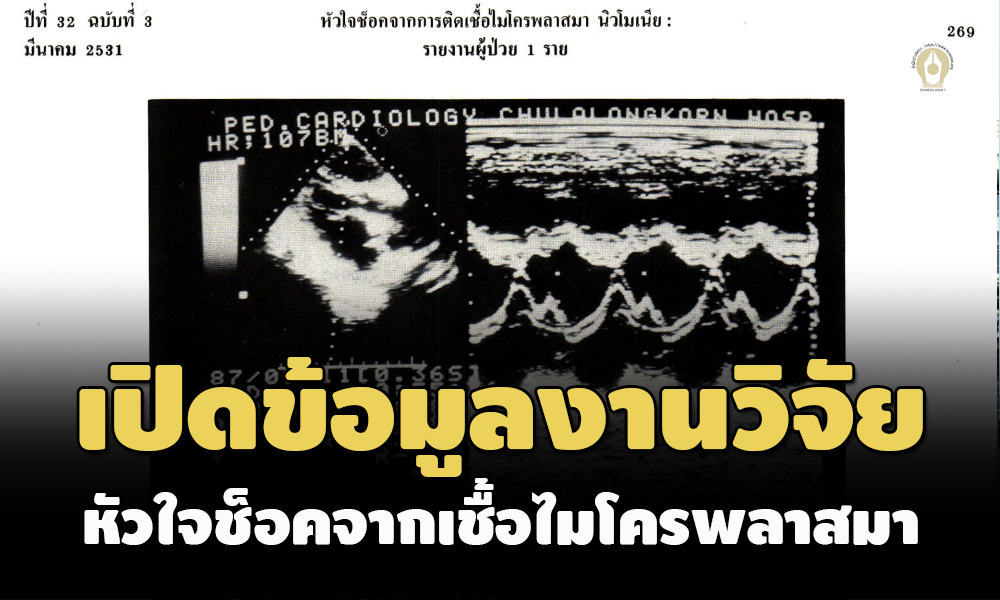
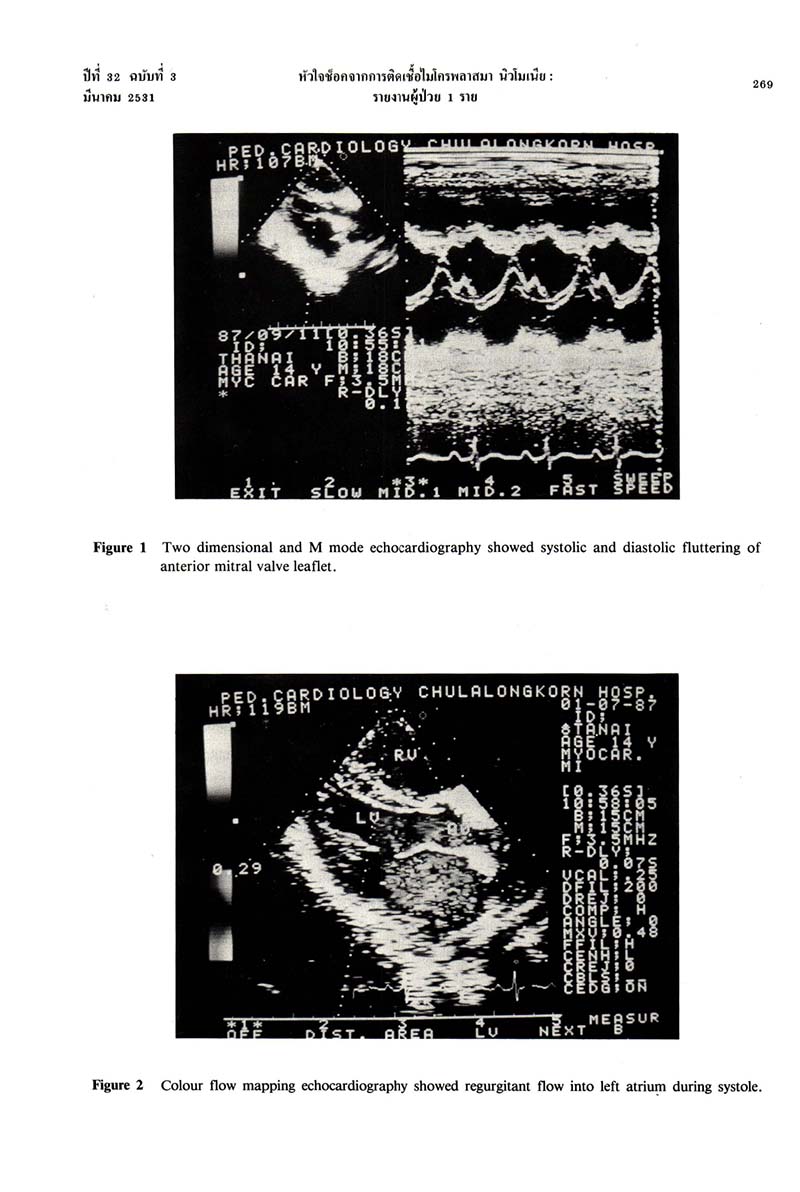
เอ็กซเรย์ปอด พบมีหัวใจโตเล็กน้อย และมี conges tion ในปอด และการตรวจคลื่นหัวใจพบมีลักษณะเป็น sinus tachycardia with first degree AV block การตรวจ ด้วย 2 D echocardiography พบมี diastolic and systolic fluttering 103 anterior mitral leaflet, noncoopture of mitral valve leaflets, dyskinesis of anterior intervent- ricular septum ไม่พบ vegetation และ pericardial effusion และจากการตรวจด้วย Doppler echocardiography และ colour flow Doppler echocardiography พบมี regurgitant flow เข้าไปใน left atrium (รูปที่ 1,2) ผู้ป่วยได้รับการรักษาด้วยยาขับปัสสาวะ ยาช่วยกล้ามเนื้อหัวใจ และ erythromycin อาการ cardiogeni shock ดีขึ้นแต่ยังมีภาวะหัวใจล้มเหลวอยู่ ต้องควบคุมด้วยการให้ยาขับปัสสาวะและยาขยายเส้นเลือด ยังคงตรวจพบมี ejection systolic murmur grade 3/6 บริเวณ apex อยู่ตลอดเวลา
วิจารณ์
ผู้ป่วยในรายงานนี้เข้ารับการรักษาในโรงพยาบาลด้วยอาการ cardiogenic shock ร่วมกับการตรวจพบว่ามี mitral insufficiency เป็นอาการนำ จําเป็นต้องวินิจฉัยแยกโรคจาก Rheumatic carditis, infective endocarditis, กล้ามเนื้อหัวใจอักเสบจากไวรัส ซึ่งจากการหาแอนติบอดี้ต่อ Gr. A สเตรปโตคอคัส ได้แก่ ASO และ anti DNase B อยู่ในระดับ ปกติและไม่มีเพิ่มขึ้นภายหลัง เช่นเดียวกับแอนติบอดีต่อ Cox- sackie B แต่พบว่าแอนติบอดีต่อ M. pneumonia โดยการ ตรวจวิธี complement fixation และการตรวจ cold agglu- tinin มีไตเตอร์ระดับสูงและมีการเพิ่มขึ้นมากกว่า 4 เท่าเมื่อ เจาะเลือดภายหลัง 2 สัปดาห์ จึงทําให้สามารถให้การวินิจฉัย ว่าเป็นการติดเชื้อ M. pneumoniae ได้ ซึ่งเข้ากับรายงาน ของผู้อื่น (1,2.3)
การติดเชื้อ M. pneumoniae พบได้บ่อยในเด็กวัยเรียนและผู้ใหญ่ ส่วนใหญ่ทําให้เกิดอาการทางระบบทางเดินหายใจ เช่น ปอดบวม หลอดลมอักเสบ น้ำในช่องปอด แต่อาจมีอาการทางระบบอื่น ๆ ร่วมด้วยได้ เช่นระบบทางเดินอาหาร โลหิต ประสาท กล้ามเนื้อ กระดูกและข้อ ผิวหนัง และหัวใจ เป็นต้น 1,2,6)
Carditis เป็นภาวะแทรกซ้อนที่สําคัญ สามารถพบ ได้ร้อยละ 2.4-8.5 ของผู้ป่วยที่มีการติดเชื้อ M. pneumoniae ผู้ป่วยส่วนใหญ่มีอายุมากกว่า 20 ปี แต่ก็มีรายงานที่พบในเด็ก อายุต่ำกว่า 1 ปี (4,6,7) ประมาณร้อยละ 70 ของผู้ป่วยเหล่านี้ จะมีอาการของการติดเชื้อที่ระบบทางเดินหายใจนํามาก่อน ประมาณ 11 วัน และประมาณร้อยละ 30 ของผู้ป่วยเหล่านี้ จะมีอาการของ carditis ภายใน 1 สัปดาห์ (6) และในบางราย มีอาการปวดกล้ามเนื้อนํามาก่อน (8) ความรุนแรงของ carditis ในผู้ป่วยแต่ละรายมีได้แตกต่างกันตั้งแต่มีเพียงความผิดปกติ ของคลื่นไฟฟ้าหัวใจ เป็นแบบ nonspecific ST-T change pericarditis, perimyocarditis, myocarditis, arrhythmia, complete AV block, หรืออาการคล้ายไข้รูห์มาติก และใน บางรายมีความรุนแรงถึงเสียชีวิต 4,6,9,13) จากการศึกษาของ Ponka ในผู้ป่วย 25 ราย พบว่าผู้ป่วย 18 ราย (72%) ตรวจพบ murmur แบบ mitral insufficiency แต่จะเป็นชั่วคราว(4) ผู้ป่วยรายนี้จากการตรวจด้วย 2D echocardiography พบมี diastolic and systolic fluttering as anterior mitral valve leaflet ufu noncoopture vos mitral valve us มี dyskinesis ของ interventricular septum การเกิด mitralinsufficiency ในผู้ป่วยรายนี้จึงน่าจะมีสาเหตุเกิดจากการมี papillary muscle dysfunction จากกล้ามเนื้อหัวใจอักเสบ และเป็นสาเหตุของการเกิด cardiogenic shock 14,15)
พยาธิสภาพกำเนิดของ carditis จาก M. pneumo-niac ยังไม่ทราบแน่ชัด เชื่อว่าอาจเกิดจากการที่เชื้อทําลาย กล้ามเนื้อหัวใจโดยตรง หรือเกิดจากกลวิธีทางอิมมูน โดย แอนติบอดี้ต่อ mycoplasma มี cross reactivity ต่อกล้ามเนื้อ หัวใจ หรือเกิดเป็น micro-thrombosis ที่ coronary artery ทําให้เกิดกล้ามเนื้อหัวใจขาดเลือด (4,11.13) จากการศึกษาของ Su-Ching-Chen ซึ่งท่า endomyocardial biopsy ในผู้ป่วย mycoplasma myocarditis ตรวจพบมี T-cell ชนิด OKT8 เป็นส่วนใหญ่ จึงทําให้เชื่อว่าการเกิด myocarditis น่าจะเกิด จากกลวิธีทางอิมมูนมากที่สุด(9)
การพยากรณ์โรคของผู้ป่วยเหล่านี้พบว่าค่อนข้างดีและมักหายเป็นปกติ แต่ในบางรายยังคงมีภาวะหัวใจล้มเหลว เรื้อรัง atrial febrillation, premature ventricular contrac tion, AV block หรือมีกล้ามเนื้อหัวใจตาย (46) และในบาง รายมีอาการรุนแรงถึงเสียชีวิต(13) แต่พบเป็นส่วนน้อย ผู้ป่วยรายนี้มีการดําเนินโรคไม่ดีนัก มีหัวใจล้มเหลวเรื้อรัง แต่ สามารถควบคุมอาการได้โดยการจํากัดการออกกําลัง การให้ยาจำพวกช่วยการทํางานของหัวใจ ยาขับปัสสาวะ และยาขยายหลอดเลือด
สรุป
ได้รายงานผู้ป่วยเด็ก 1 ราย ซึ่งเข้ารับการรักษาด้วยอาการ cardiogenic shock และ mitral insufficiency จากการตรวจทางห้องปฏิบัติการพบว่าผู้ป่วยมีการติดเชื้อ M. pne umoniae และสาเหตุของ mitral insufficiency เกิดจาก การมี papillary muscle dysfunction จากการมีทำลายต่อ กล้ามเนื้อหัวใจ ดังนั้นในผู้ป่วยที่มีอาการของหัวใจวายเฉียบพลันร่วมกับ mitral insufficiency จําเป็นต้องคิดถึงสาเหตุ จากการติดเชื้อ M. pneumoniae นอกเหนือจากไข้รูห์มาติก กล้ามเนื้อหัวใจอักเสบจากเชื้อไวรัส และ การติดเชื้อที่ลิ้นหัวใจ






 Isranews Agency | สำนักข่าวอิศรา
Isranews Agency | สำนักข่าวอิศรา